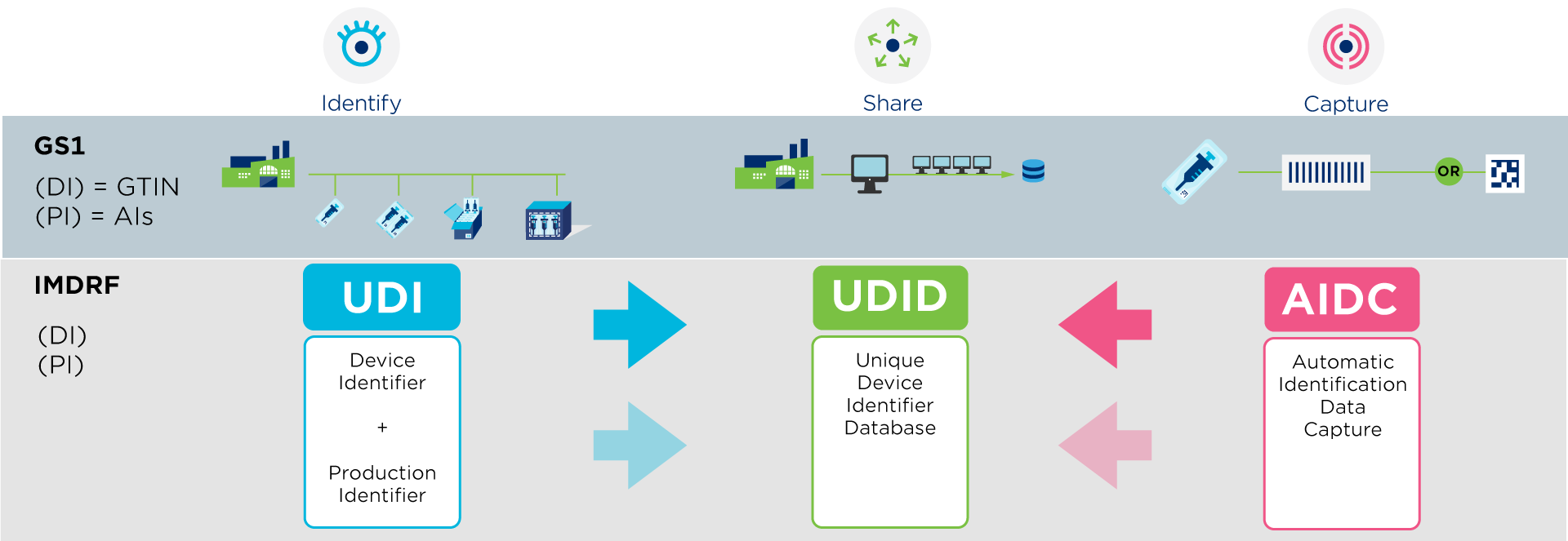
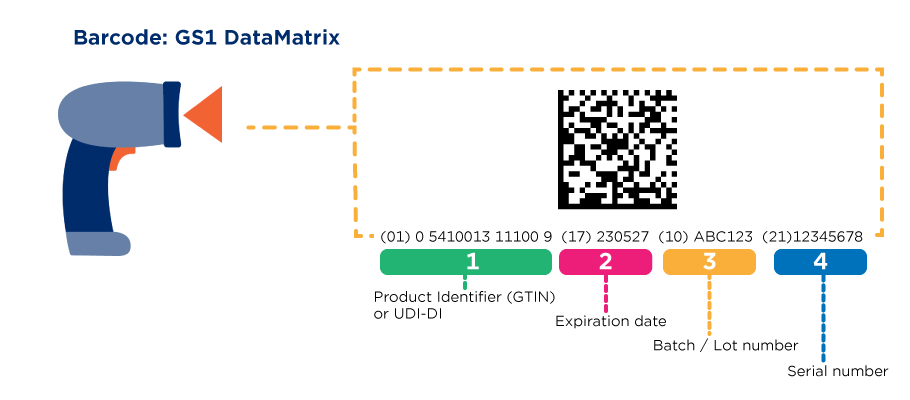
Een UDI (Unique Device Identifier) is een wereldwijd unieke code die gebruikt wordt om medische hulpmiddelen te identificeren. De code bestaat uit een vast gedeelte (de Device Identifier of DI) en een variabel gedeelte (Product Identifier of PI). Hierbij kunnen zowel numerieke als alfanumerieke tekens worden gebruikt.
GS1 is een geaccrediteerde UDI-uitgevende organisatie die je helpt te voldoen aan de internationale regelgeving, zoals EU MDR & IVDR en US FDA, die vereist dat leveranciers een UDI aan hun producten toekennen.

Als leverancier ben je verplicht om je gegevens (=UDI-DI) te registreren in een gereguleerde database van de overheid.
Voor Amerika (FDA) is dat GUDID en kan je vanuit My Product Manager je UDI-DI hier naartoe publiceren.
Voor Europa is dat EUDAMED. Deze gegevens kan je via My Basic UDI-DI Manager publiceren. Stuur een e-mail naar healthcare@gs1belu.org moest je hier interesse in hebben.