Een UDI (Unique Device Identifier) is een wereldwijd unieke code die dient om medische hulpmiddelen te identificeren. Een UDI bestaat uit twee onderdelen:
- UDI-DI (Device Identifier of DI): Het vaste deel van de code dat elk medisch hulpmiddel uniek identificeert via een GTIN
- UDI-PI (Production Identifier of PI): Het variabele deel dat productie-informatie toevoegt, zoals lotnummer, serienummer of vervaldatum.
Internationale regelgeving, zoals de MDR en IVDR in Europa en de FDA-richtlijnen in de Verenigde Staten, verplicht leveranciers om voor alle medische hulpmiddelen een UDI toe te wijzen.
GS1 is een geaccrediteerde UDI-uitgevende organisatie die je helpt te voldoen aan de internationale regelgeving, zoals EU MDR & IVDR en US FDA, die vereist dat leveranciers een UDI aan hun producten toekennen.
In Europa wordt de UDI-DI ook gebruikt om de Basic UDI-DI te vormen.

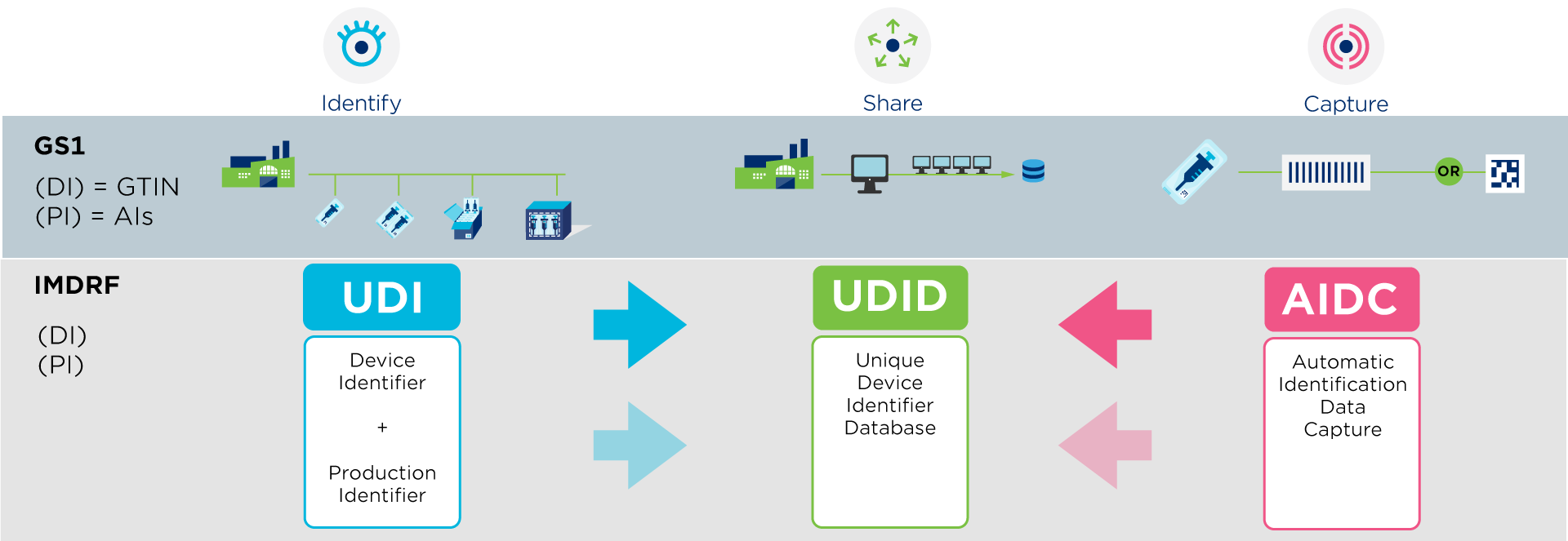
Naleving van de UDI voorschriften voor medische hulpmiddelen is gebaseerd op 3 principes, zoals vastgelegd door het International Medical Device Regulators Forum (IMDRF). Deze wereldwijde richtlijnen vormen de basis voor nationale wetgeving, zodat elke regio kan voldoen aan haar specifieke vereisten.
- Identificatie van medische hulpmiddelen door middel van een UDI.
- De mogelijkheid om via een barcode de informatie te scannen, zo zijn de GS1 DataMatrix en de GS1-128 barcode toegelaten in de Europese Unie en vervatten die alle informatie die wettelijk vereist is in één barcode.
- Het delen van de productinformatie in een reglementaire database, zoals EUDAMED voor de Europese Unie of GUDID in de Verenigde Staten.