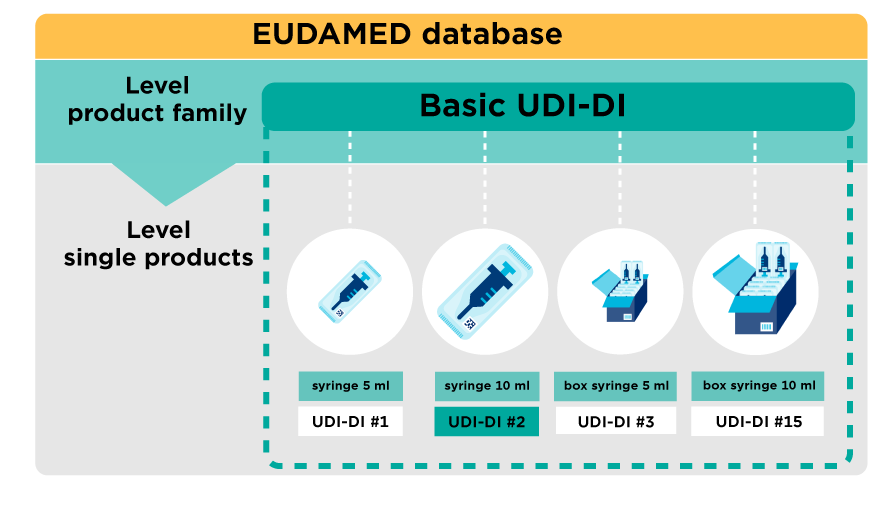
En tant que fabricant de dispositifs médicaux, vous avez déjà attribué des identifiants uniques des dispositifs (UDI-DI) à vos produits. Pour la Medical Device Regulation (MDR) etl' In-Vitro Diagnostic Regulation (IVDR), ces produits doivent maintenant aussi être enregistrés dans EUDAMED au moyen de Basic UDI-DI. Cela se fait facilement avec My Basic UDI-DI Manager.
My Basic UDI-DI Manager est la solution de GS1 Belgium & Luxembourg pour :
- Créer et/ou gérer facilement vos Basic UDI-DI ou Global Model Number (GMN) ;
- Remplir les données requises par EUDAMED selon les caractéristiques du produit ;
- Lier les numéros d’identification uniques de vos dispositifs médicaux UDI-DI (ou GTIN) avec votre Basic UDI-DI ou GMN ;
- Publier les informations facilement vers EUDAMED avec feedback intégré d'EUDAMED selon les MDR et IVDR.
Pour utiliser My Basic UDI-DI Manager, vous devez souscrire un abonnement payant à My Product Manager Share et My Basic UDI-DI Manager.